Regulatory affairs inom life sciences

Regulatory affairs inom life sciences är en av de mest komplexa och ständigt föränderliga delarna av läkemedels- och bioteknikindustrin. I och med den snabba utvecklingen av nya terapier och innovationer, spelar regulatory affairs en kritisk roll för att säkerställa att produkter inte bara uppfyller säkerhets- och effektivitetskraven utan också följer regionala och internationella bestämmelser. Denna artikel dyker in i hur regulatory affairs fungerar, vilka utmaningar som möter aktörerna inom området och hur företag som MaxRegConsult kan hjälpa till att navigera i denna komplexa miljö.
Förståelse för regulatory affairs
Regulatory affairs handlar om processen att utveckla, registrera och korrekt kommersialisera medicinska produkter under strikta regler och bestämmelser. Detta inkluderar läkemedel, bioteknologiprodukter, medicintekniska produkter och ibland även livsmedelstillsatser. Arbetet innebär en kontinuerlig dialog med myndigheter, som Läkemedelsverket i Sverige eller EMA i Europa, för att säkerställa att alla produkter som går ut på marknaden är säkra och effektiva för konsumenterna.
En central del av regulatory affairs är att tolka och implementera internationella riktlinjer och bestämmelser. Detta kräver en djup förståelse för komplexa forskningsdata och kräver ofta samarbete mellan olika discipliner inklusive vetenskap, juridik och marknadsföring. Att misslyckas med att följa gällande lagar kan leda till tillbakadragande av produkter från marknaden, vilket kan resultera i betydande ekonomiska förluster för företaget.
Vanliga utmaningar inom regulatory affairs
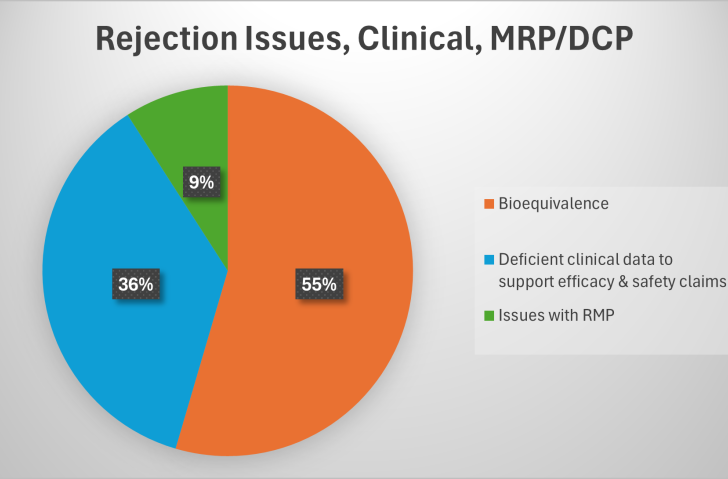
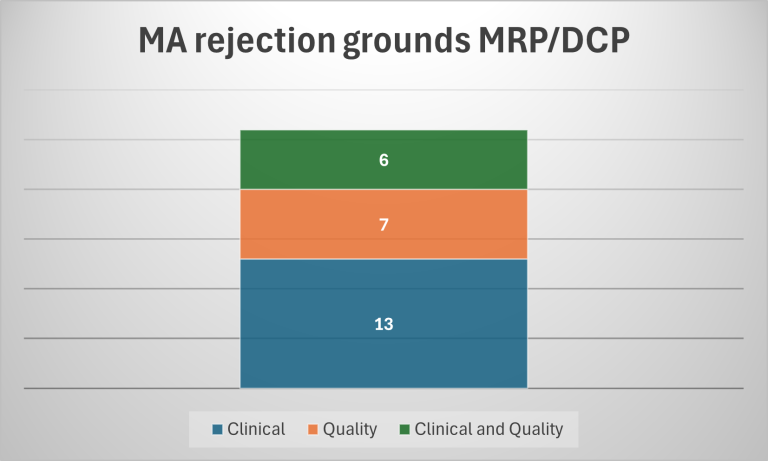
Inom regulatory affairs finns det flera utmaningar som företag måste hantera. En av de mest kritiska är hanteringen av avslag på marknadsföringstillstånd. Ett avslag kan vara mycket smärtsamt för företag eftersom det innebär att stora mängder tid och resurser som investerats kan vara bortkastade. Enligt en analys av MaxRegConsult, har bioekvivalens varit en vanlig anledning till avslag inom MRP/DCP-förfaranden. Problemet ligger ofta i svårigheten att visa att en ny produkt är likvärdig med en referensprodukt, vilket särskilt påverkar generiska läkemedelsföretag.
Kvalitetsfrågor är en annan utmaning, där problem kan uppstå med allt från stabilitetstester till nitrosaminprovning. Dessa problem kan vara komplexa och kräver en djupgående analys och förståelse för att lösa. Hastigheten som nya riktlinjer och krav implementeras med förändrar dessutom ständigt landskapet, vilket gör det avgörande för företag att hålla sig uppdaterade för att undvika motgångar.
Lösningar och expertstöd
För att navigera i denna komplicerade värld, behöver företag rätt stöd och resurser för att lyckas. MaxRegConsult är en av de aktörer som erbjuder skräddarsydda lösningar för företag inom life sciences. De tillhandahåller expertis i allt från mindre projekt till fullständig insourcing, vilket ger företag den flexibilitet som krävs för att säkerställa att de förblir i linje med aktuella regler och standarder.
MaxRegConsult erbjuder också insikter för att minimera risken för avslag vid ansökningar om marknadsföringstillstånd. Genom sina djupgående analyser och strategiska vägledning hjälper de företag att effektivt demonstrera bioekvivalens och hantera kvalitetsfrågor på ett smidigt sätt, för att undvika kostsamma avslag och fördröjningar. Med en gedigen erfarenhet tar de sig an allt från dokumentförfattande till marknadsföringskampanjer, och hjälper företag att växa utan att kompromissa med efterlevnad.





















